مؤلف:
Joan Hall
تاريخ الخلق:
28 شهر فبراير 2021
تاريخ التحديث:
1 تموز 2024

المحتوى
- خطوات
- طريقة 1 من 3: إيجاد الكتلة الذرية باستخدام الجدول الدوري للعناصر
- طريقة 2 من 3: حساب الكتلة الذرية لذرة واحدة
- طريقة 3 من 3: حساب الكتلة الذرية النسبية (الوزن الذري) لعنصر
- نصائح
- ماذا تحتاج
الكتلة الذرية هو مجموع كتل كل البروتونات والنيوترونات والإلكترونات التي تتكون منها هذه الذرة أو الجزيء. بالمقارنة مع البروتونات والنيوترونات ، فإن كتلة الإلكترونات صغيرة جدًا ، لذلك لا يتم أخذها في الاعتبار في الحسابات. على الرغم من أن هذا غير صحيح من وجهة نظر رسمية ، إلا أن هذا المصطلح يستخدم غالبًا للإشارة إلى متوسط الكتلة الذرية لجميع نظائر العنصر. في الواقع ، هذه هي الكتلة الذرية النسبية ، وتسمى أيضًا الوزن الذري جزء. الوزن الذري هو متوسط الكتل الذرية لجميع نظائر عنصر ما بشكل طبيعي. يجب على الكيميائيين التمييز بين هذين النوعين من الكتلة الذرية عند القيام بعملهم - يمكن أن تؤدي قيمة الكتلة الذرية غير الصحيحة ، على سبيل المثال ، إلى نتيجة غير صحيحة لعائد منتج التفاعل.
خطوات
طريقة 1 من 3: إيجاد الكتلة الذرية باستخدام الجدول الدوري للعناصر
 1 تعلم كيف تكتب الكتلة الذرية. يمكن التعبير عن الكتلة الذرية ، أي كتلة ذرة أو جزيء معين ، بوحدات SI القياسية - جرامات ، كيلوجرام ، وما إلى ذلك. ومع ذلك ، نظرًا لحقيقة أن الكتل الذرية المعبر عنها في هذه الوحدات صغيرة للغاية ، فغالبًا ما يتم تسجيلها في وحدات كتلة ذرية موحدة ، أو مختصرة amu. - وحدات الكتلة الذرية. وحدة كتلة ذرية واحدة تساوي 1/12 من كتلة النظير القياسي كربون -12.
1 تعلم كيف تكتب الكتلة الذرية. يمكن التعبير عن الكتلة الذرية ، أي كتلة ذرة أو جزيء معين ، بوحدات SI القياسية - جرامات ، كيلوجرام ، وما إلى ذلك. ومع ذلك ، نظرًا لحقيقة أن الكتل الذرية المعبر عنها في هذه الوحدات صغيرة للغاية ، فغالبًا ما يتم تسجيلها في وحدات كتلة ذرية موحدة ، أو مختصرة amu. - وحدات الكتلة الذرية. وحدة كتلة ذرية واحدة تساوي 1/12 من كتلة النظير القياسي كربون -12. - وحدة الكتلة الذرية تميز الكتلة مول واحد من عنصر معين بالجرام... هذه القيمة مفيدة جدًا في الحسابات العملية ، حيث يمكن استخدامها بسهولة لتحويل كتلة عدد معين من ذرات أو جزيئات مادة معينة إلى مولات ، والعكس صحيح.
 2 أوجد الكتلة الذرية في الجدول الدوري. تحتوي معظم الجداول الدورية القياسية على الكتل الذرية (الأوزان الذرية) لكل عنصر. كقاعدة عامة ، يتم عرضها كرقم في أسفل الخلية مع العنصر ، أسفل الأحرف التي تشير إلى العنصر الكيميائي. هذا ليس عادةً عددًا صحيحًا ، ولكنه كسر عشري.
2 أوجد الكتلة الذرية في الجدول الدوري. تحتوي معظم الجداول الدورية القياسية على الكتل الذرية (الأوزان الذرية) لكل عنصر. كقاعدة عامة ، يتم عرضها كرقم في أسفل الخلية مع العنصر ، أسفل الأحرف التي تشير إلى العنصر الكيميائي. هذا ليس عادةً عددًا صحيحًا ، ولكنه كسر عشري. - لاحظ أن جميع الكتل الذرية النسبية الواردة في الجدول الدوري لكل عنصر هي معدل القيم. العناصر الكيميائية مختلفة النظائر - الأنواع الكيميائية التي لها كتل مختلفة بسبب النيوترونات الإضافية أو المفقودة في نواة الذرة. لذلك ، يمكن استخدام الكتل الذرية النسبية المدرجة في الجدول الدوري كمتوسط لذرات عنصر معين ، ولكن ليس ككتلة ذرة واحدة من عنصر معين.
- تُستخدم الكتل الذرية النسبية الواردة في الجدول الدوري لحساب الكتل المولية للذرات والجزيئات. معبراً عن الكتل الذرية بوحدة amu (كما في الجدول الدوري) هي في الأساس بلا أبعاد. ومع ذلك ، ببساطة بضرب الكتلة الذرية في 1 جم / مول ، نحصل على خاصية مفيدة لعنصر - الكتلة (بالجرام) لمول واحد من ذرات هذا العنصر.
 3 تذكر أن الجدول الدوري يسرد متوسط الكتل الذرية للعناصر. كما ذكرنا سابقًا ، فإن الكتل الذرية النسبية المشار إليها لكل عنصر في الجدول الدوري هي متوسط كتل جميع النظائر في الذرة. هذا المتوسط ذو قيمة للعديد من الأغراض العملية: على سبيل المثال ، يتم استخدامه لحساب الكتلة المولية للجزيئات المكونة من عدة ذرات. ومع ذلك ، عندما تتعامل مع ذرات منفردة ، فإن هذه القيمة لا تكفي عادة.
3 تذكر أن الجدول الدوري يسرد متوسط الكتل الذرية للعناصر. كما ذكرنا سابقًا ، فإن الكتل الذرية النسبية المشار إليها لكل عنصر في الجدول الدوري هي متوسط كتل جميع النظائر في الذرة. هذا المتوسط ذو قيمة للعديد من الأغراض العملية: على سبيل المثال ، يتم استخدامه لحساب الكتلة المولية للجزيئات المكونة من عدة ذرات. ومع ذلك ، عندما تتعامل مع ذرات منفردة ، فإن هذه القيمة لا تكفي عادة. - نظرًا لأن متوسط الكتلة الذرية هو متوسط القيمة للعديد من النظائر ، فإن القيمة الموضحة في الجدول الدوري ليست كذلك دقيق قيمة الكتلة الذرية لأي ذرة مفردة.
- يجب حساب الكتل الذرية للذرات الفردية مع الأخذ في الاعتبار العدد الدقيق للبروتونات والنيوترونات في ذرة واحدة.
طريقة 2 من 3: حساب الكتلة الذرية لذرة واحدة
 1 أوجد العدد الذري لعنصر معين أو نظيره. العدد الذري هو عدد البروتونات في ذرات العنصر ، ولا يتغير أبدًا. على سبيل المثال ، كل ذرات الهيدروجين و فقط لديهم بروتون واحد. العدد الذري للصوديوم هو 11 ، لأن نواتها بها أحد عشر بروتونًا ، بينما العدد الذري للأكسجين هو ثمانية ، لأن نواتها بها ثمانية بروتونات. يمكنك العثور على العدد الذري لأي عنصر في الجدول الدوري لمندلييف - في جميع إصداراته القياسية تقريبًا ، يشار إلى هذا الرقم أعلى التعيين الحرفي للعنصر الكيميائي. العدد الذري دائمًا عدد صحيح موجب.
1 أوجد العدد الذري لعنصر معين أو نظيره. العدد الذري هو عدد البروتونات في ذرات العنصر ، ولا يتغير أبدًا. على سبيل المثال ، كل ذرات الهيدروجين و فقط لديهم بروتون واحد. العدد الذري للصوديوم هو 11 ، لأن نواتها بها أحد عشر بروتونًا ، بينما العدد الذري للأكسجين هو ثمانية ، لأن نواتها بها ثمانية بروتونات. يمكنك العثور على العدد الذري لأي عنصر في الجدول الدوري لمندلييف - في جميع إصداراته القياسية تقريبًا ، يشار إلى هذا الرقم أعلى التعيين الحرفي للعنصر الكيميائي. العدد الذري دائمًا عدد صحيح موجب. - لنفترض أننا مهتمون بذرة كربون. يوجد دائمًا ستة بروتونات في ذرات الكربون ، لذلك نعلم أن عددها الذري هو 6. بالإضافة إلى ذلك ، نرى أنه في الجدول الدوري ، يوجد في الجزء العلوي من الخلية مع الكربون (C) الرقم "6" ، مما يشير إلى أن عدد الكربون الذري هو ستة.
- لاحظ أن العدد الذري لعنصر ما لا يرتبط بشكل فريد بكتلته الذرية النسبية في الجدول الدوري. على الرغم من أنه ، خاصة بالنسبة للعناصر الموجودة أعلى الجدول ، قد يبدو أن الكتلة الذرية لعنصر ما هي ضعف العدد الذري ، إلا أنه لا يتم حسابها أبدًا بضرب الرقم الذري في اثنين.
 2 أوجد عدد النيوترونات في النواة. يمكن أن يختلف عدد النيوترونات باختلاف ذرات نفس العنصر. عندما تمتلك ذرتان من نفس العنصر لهما نفس عدد البروتونات عددًا مختلفًا من النيوترونات ، فإنهما نظائر مختلفة لهذا العنصر.على عكس عدد البروتونات ، الذي لا يتغير أبدًا ، يمكن أن يتغير عدد النيوترونات في ذرات عنصر معين غالبًا ، لذلك تتم كتابة متوسط الكتلة الذرية لعنصر ما على هيئة كسر عشري بقيمة تقع بين عددين صحيحين متجاورين.
2 أوجد عدد النيوترونات في النواة. يمكن أن يختلف عدد النيوترونات باختلاف ذرات نفس العنصر. عندما تمتلك ذرتان من نفس العنصر لهما نفس عدد البروتونات عددًا مختلفًا من النيوترونات ، فإنهما نظائر مختلفة لهذا العنصر.على عكس عدد البروتونات ، الذي لا يتغير أبدًا ، يمكن أن يتغير عدد النيوترونات في ذرات عنصر معين غالبًا ، لذلك تتم كتابة متوسط الكتلة الذرية لعنصر ما على هيئة كسر عشري بقيمة تقع بين عددين صحيحين متجاورين. - يمكن تحديد عدد النيوترونات من خلال تعيين نظير العنصر. على سبيل المثال ، الكربون 14 هو نظير مشع طبيعي للكربون 12. غالبًا ما يُشار إلى الرقم النظيري كرقم مرتفع أمام رمز العنصر: ج. يمكن إيجاد عدد النيوترونات بطرح عدد البروتونات من العدد النظيري: 14-6 = 8 نيوترونات.
- لنفترض أن ذرة الكربون المعنية بها ستة نيوترونات (C). إنه أكثر نظائر الكربون وفرة ، حيث يمثل حوالي 99 ٪ من جميع ذرات هذا العنصر. ومع ذلك ، فإن حوالي 1٪ من ذرات الكربون تحتوي على 7 نيوترونات (C). تحتوي الأنواع الأخرى من ذرات الكربون على أكثر من 7 أو أقل من 6 نيوترونات وتوجد بكميات صغيرة جدًا.
 3 اجمع عدد البروتونات والنيوترونات. ستكون هذه هي الكتلة الذرية للذرة المعينة. تجاهل عدد الإلكترونات التي تحيط بالنواة - كتلتها الكلية صغيرة جدًا ، لذا فهي عمليًا لا تؤثر على حساباتك.
3 اجمع عدد البروتونات والنيوترونات. ستكون هذه هي الكتلة الذرية للذرة المعينة. تجاهل عدد الإلكترونات التي تحيط بالنواة - كتلتها الكلية صغيرة جدًا ، لذا فهي عمليًا لا تؤثر على حساباتك. - تحتوي ذرة الكربون لدينا على 6 بروتونات + 6 نيوترونات = 12. وبالتالي ، فإن الكتلة الذرية لذرة الكربون هذه هي 12. إذا كان هذا هو النظير "الكربون -13" ، فسنعرف أن لديها 6 بروتونات + 7 نيوترونات = الوزن الذري 13.
- في الواقع ، الكتلة الذرية للكربون 13 هي 13.003355 ، وهذه القيمة أكثر دقة ، حيث تم تحديدها تجريبيًا.
- الكتلة الذرية قريبة جدًا من عدد النظائر. لتسهيل العمليات الحسابية ، غالبًا ما يُفترض أن عدد النظائر يساوي الكتلة الذرية. تتجاوز القيم المحددة تجريبياً للكتلة الذرية عدد النظائر قليلاً بسبب المساهمة الصغيرة جدًا من الإلكترونات.
طريقة 3 من 3: حساب الكتلة الذرية النسبية (الوزن الذري) لعنصر
 1 تحديد النظائر الموجودة في العينة. غالبًا ما يحدد الكيميائيون نسبة النظائر في عينة معينة باستخدام أداة خاصة تسمى مطياف الكتلة. ومع ذلك ، أثناء التدريب ، سيتم توفير هذه البيانات لك في ظروف المهام والرقابة وما إلى ذلك في شكل قيم مأخوذة من الأدبيات العلمية.
1 تحديد النظائر الموجودة في العينة. غالبًا ما يحدد الكيميائيون نسبة النظائر في عينة معينة باستخدام أداة خاصة تسمى مطياف الكتلة. ومع ذلك ، أثناء التدريب ، سيتم توفير هذه البيانات لك في ظروف المهام والرقابة وما إلى ذلك في شكل قيم مأخوذة من الأدبيات العلمية. - في حالتنا ، لنفترض أننا نتعامل مع نظيرين: كربون -12 وكربون -13.
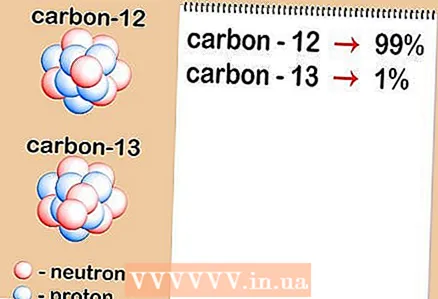 2 تحديد المحتوى النسبي لكل نظير في العينة. لكل عنصر ، تحدث نظائر مختلفة بنسب مختلفة. يتم التعبير عن هذه النسب دائمًا كنسب مئوية. بعض النظائر شائعة جدًا ، في حين أن البعض الآخر نادر جدًا - يصعب اكتشافه في بعض الأحيان. يمكن تحديد هذه الكميات باستخدام مطياف الكتلة أو يمكن العثور عليها في كتيب.
2 تحديد المحتوى النسبي لكل نظير في العينة. لكل عنصر ، تحدث نظائر مختلفة بنسب مختلفة. يتم التعبير عن هذه النسب دائمًا كنسب مئوية. بعض النظائر شائعة جدًا ، في حين أن البعض الآخر نادر جدًا - يصعب اكتشافه في بعض الأحيان. يمكن تحديد هذه الكميات باستخدام مطياف الكتلة أو يمكن العثور عليها في كتيب. - لنفترض أن تركيز الكربون -12 هو 99٪ ، والكربون -13 هو 1٪. نظائر الكربون الأخرى حقا موجودة ، ولكن بكميات صغيرة جدًا بحيث يمكن إهمالها في هذه الحالة.
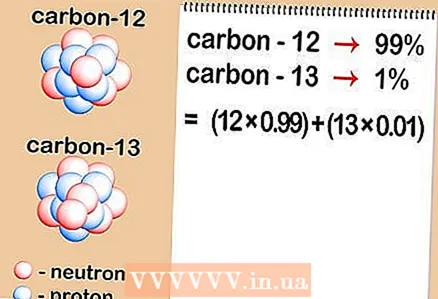 3 اضرب الكتلة الذرية لكل نظير في تركيزه في العينة. اضرب الكتلة الذرية لكل نظير في نسبته المئوية (معبرًا عنها في صورة كسر عشري). لتحويل النسب المئوية إلى كسور عشرية ، اقسم ببساطة على 100. يجب أن تضيف التركيزات الناتجة دائمًا ما يصل إلى 1.
3 اضرب الكتلة الذرية لكل نظير في تركيزه في العينة. اضرب الكتلة الذرية لكل نظير في نسبته المئوية (معبرًا عنها في صورة كسر عشري). لتحويل النسب المئوية إلى كسور عشرية ، اقسم ببساطة على 100. يجب أن تضيف التركيزات الناتجة دائمًا ما يصل إلى 1. - تحتوي عينتنا على كربون -12 وكربون -13. إذا كان الكربون -12 يمثل 99٪ من العينة ، والكربون -13 يمثل 1٪ ، فمن الضروري ضرب 12 (الكتلة الذرية للكربون -12) في 0.99 و 13 (الكتلة الذرية للكربون -13) في 0.01.
- تعطي الكتب المرجعية النسب المئوية بناءً على الكميات المعروفة لجميع نظائر العنصر. تحتوي معظم كتب الكيمياء المدرسية على هذه المعلومات في شكل جداول في نهاية الكتاب. بالنسبة للعينة قيد الدراسة ، يمكن أيضًا تحديد التركيزات النسبية للنظائر باستخدام مطياف الكتلة.
 4 اجمع النتائج. لخص نتائج الضرب التي حصلت عليها في الخطوة السابقة.كنتيجة لهذه العملية ، ستجد الكتلة الذرية النسبية للعنصر - متوسط قيمة الكتل الذرية لنظائر العنصر المعني. عند النظر إلى عنصر ككل ، بدلاً من نظير معين لعنصر معين ، فإن هذه القيمة هي المستخدمة.
4 اجمع النتائج. لخص نتائج الضرب التي حصلت عليها في الخطوة السابقة.كنتيجة لهذه العملية ، ستجد الكتلة الذرية النسبية للعنصر - متوسط قيمة الكتل الذرية لنظائر العنصر المعني. عند النظر إلى عنصر ككل ، بدلاً من نظير معين لعنصر معين ، فإن هذه القيمة هي المستخدمة. - في مثالنا ، 12 × 0.99 = 11.88 للكربون -12 ، و 13 × 0.01 = 0.13 للكربون -13. الكتلة الذرية النسبية في حالتنا هي 11.88 + 0.13 = 12,01.
نصائح
- بعض النظائر أقل ثباتًا من غيرها: فهي تتحلل إلى ذرات من عناصر تحتوي على عدد أقل من البروتونات والنيوترونات في النواة ، وتطلق الجزيئات التي تشكل النواة الذرية. تسمى هذه النظائر المشعة.
ماذا تحتاج
- كتيب الكيمياء
- آلة حاسبة



