مؤلف:
Monica Porter
تاريخ الخلق:
17 مارس 2021
تاريخ التحديث:
1 تموز 2024

المحتوى
يشير التركيز المولي إلى العلاقة بين عدد مولات المذاب وحجم المحلول. لحساب المولارية ، يمكنك البدء بالمولات والحجم والكتلة والحجم أو المولات والمليليترات (مل). بعد ذلك ، باستخدام المتغيرات المذكورة أعلاه ، قم بتطبيق صيغة التركيز المولي الأساسية للحصول على النتيجة الصحيحة.
خطوات
الطريقة 1 من 4: حساب تركيز المول من الرقم المولي والحجم
من المهم معرفة الصيغة الأساسية لحساب التركيز المولي. التركيز المولي يساوي عدد مولات المذاب مقسومًا على حجم المحلول باللترات. من هناك ، لدينا الصيغة التالية: التركيز المولي = عدد مولات المذاب / عدد لترات المحلول
- مثال: ما هو التركيز المولي لمحلول يحتوي على 0.75 مول كلوريد الصوديوم في 4.2 لتر من المحلول؟

حلل الموضوع. لحساب التركيز المولي ، تحتاج إلى عدد المولات وحجم المحلول باللترات. لا تحتاج إلى حساب هاتين القيمتين بسبب الموضوع المحدد.- فمثلا:
- عدد المولات = 0.75 مول من كلوريد الصوديوم
- الحجم = 4.2 لتر
- فمثلا:
اقسم عدد المولات على الحجم. نتيجة قسمة الخلد حسب الحجم هي عدد المولات لكل لتر من المحلول أو التركيز المولي لهذا المحلول.
- مثال: التركيز المولي = عدد مولات المذاب / عدد لترات المحلول = 0.75 مول / 4.2 لتر = 0.17857142

سجل نتائجك. قم بالتقريب إلى رقمين أو ثلاثة أرقام بعد الفاصلة ، بناءً على طلب المعلم أو الواجب. عند تسجيل نتائجك ، اختصر "التركيز المولي" بـ "M" وقم بتضمين الرمز الكيميائي للمذاب.- فمثلا: 0.179 م كلوريد الصوديوم
طريقة 2 من 4: حساب تركيز المول من الكتلة والحجم
من الضروري معرفة الصيغة الأساسية لحساب التركيز المولي. يوضح التركيز المولي العلاقة بين عدد مولات المذاب وحجم المحلول. صيغة التركيز المولي هي كما يلي: التركيز المولي = تركيز المذاب / عدد لترات المحلول
- مثال المشكلة: احسب عدد مولات المحلول عند إذابة 3.4 جم من KMnO4 في 5.2 لتر من الماء.

حلل الموضوع: لإيجاد التركيز المولي ، تحتاج إلى عدد المولات وحجم المحلول باللترات. إذا لم يتم إعطاء هذه القيم ، لكنك تعرف حجم وكتلة المحلول ، يمكنك تحديد عدد مولات المذاب قبل حساب التركيز المولي.- فمثلا:
- الوزن = 3.4 جم KMnO4
- الحجم = 5.2 لتر
- فمثلا:
احسب جزيء الكتلة للمذاب. لحساب عدد مولات المذاب من تلك الكتلة أو جرامات المذاب ، عليك أولاً تحديد جزيء الكتلة للمذاب. يمكن تحديد جزيء الكتلة للمذاب عن طريق إضافة ذرة الكتلة لكل عنصر في المحلول. لإيجاد الذرة المكعبة لكل عنصر ، استخدم الجدول الدوري للعناصر.
- فمثلا:
- ذرة كتلة K = 39.1 جم
- كتلة ذرة Mn = 54،9 جم
- ذرة كتلة O = 16.0 جم
- مجموع ذرات الكتلة = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 جرام
- فمثلا:
حول الجرامات إلى مولات. بمجرد حصولك على جزيء مكعب ، ستحتاج إلى ضرب عدد جرامات المذاب في المحلول بمعامل التحويل المكافئ 1 مول لكل كتلة مولية للمذاب. نتيجة هذا الضرب هي عدد مولات المذاب.
- مثال: غرام من المذاب * (1 / الكتلة المولية للمذاب) = 3.4 جم * (1 مول / 158 جم) = 0.0215 مول
اقسم عدد المولات على عدد اللترات. الآن بعد أن قمت بحساب عدد المولات ، اقسم الآن هذا الرقم على حجم المحلول باللترات ، سيكون لديك التركيز المولي لهذا المحلول.
- مثال: التركيز المولي = عدد مولات المذاب / عدد لترات المحلول = 0.0215 مول / 5.2 لتر = 0.004134615
سجل نتائجك. تحتاج إلى تقريب النتائج كما هو مطلوب من قبل المعلم ، وعادة ما تكون من رقمين إلى ثلاثة أرقام بعد الفاصلة. بالإضافة إلى ذلك ، عند كتابة النتيجة ، اختصر "التركيز المولي" كـ "M" ورافق الرمز الكيميائي للمذاب.
- فمثلا: 0.004 م KMnO4
طريقة 3 من 4: احسب التركيز المولي من عدد المولات والمليليترات من المحلول
بحاجة إلى معرفة صيغة التركيز المولي. لحساب التركيز المولي. تحتاج إلى حساب عدد مولات المذاب لكل لتر من المحلول ، وليس عدد مولات المحلول. الصيغة العامة لحساب التركيز المولي هي: التركيز المولي = عدد مولات المذاب / عدد لترات المحلول
- مثال: احسب التركيز المولي لمحلول يحتوي على 1.2 مول من CaCl2 في 2905 مليلتر من الماء.
حلل الموضوع. لحساب التركيز المولي ، تحتاج إلى عدد مولات المذاب وحجم المحلول باللترات. إذا تم إعطاء حجم الحل في المشكلة بالملليترات ، فأنت بحاجة إلى التحويل إلى الحجم المكافئ باللترات قبل إجراء الحساب.
- فمثلا:
- عدد الشامات = 1.2 مول من CaCl2
- الحجم = 2905 مل
- فمثلا:
حول المليلتر إلى لتر. لتحويل المحلول من مليلتر إلى لتر ، اقسم عدد المليلتر على 1000 ، لأن كل لتر يساوي 1000 مليلتر. يمكنك أيضًا تحويل الملليمترات إلى لترات عن طريق تحويل العلامة العشرية إلى اليسار بمقدار 3 أرقام.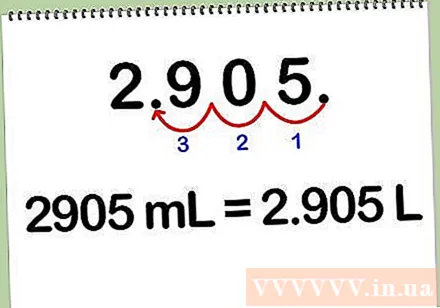
- على سبيل المثال: 2905 مل * (1 لتر / 1000 مل) = 2905 لتر
اقسم عدد المولات على عدد اللترات. بعد أن يكون لديك عدد اللترات ، يمكنك حساب التركيز المولي بقسمة عدد المولات على عدد لترات المحلول.
- مثال: التركيز المولي = عدد مولات المذاب / عدد لترات المحلول = 1.2 مول من CaCl2 / 2905 لتر = 0.413080895
سجل نتائجك. تذكر تقريب النتيجة إلى فاصلتين أو ثلاث ، أو حسب طلب معلمك. عند تسجيل النتيجة ، اختصر "التركيز المولي" كـ "M" ثم الرمز الكيميائي للمذاب.
- فمثلا: 0.413 م كاكل2
طريقة 4 من 4: تمرين إضافي
احسب التركيز المولي لمحلول عندما يذوب 5.2 جم كلوريد الصوديوم في 800 مل من الماء. حدد القيم المعطاة في المسألة: الكتلة بالجرام والحجم بالملليلترات.
- الكتلة = 5.2 جم كلوريد الصوديوم
- الحجم = 800 مل من الماء
أوجد جزيء الكتلة لكلوريد الصوديوم بإضافة الذرة المكعبة للعنصر Na وذرة الكتلة Cl.
- كتلة ذرة Na = 22.99 جم
- ذرة الكتلة Cl = 35.45 جم
- جزيئات الكتلة من NaCl = 22.99 + 35.45 = 58.44 جم
اضرب كتلة المذاب في معامل التحويل المولي. في هذا المثال ، الكتلة الجزيئية لـ NaCl هي 58.44 جم ، وبالتالي فإن عامل التحويل هو "1 مول / 58.44 جم".
- عدد مول كلوريد الصوديوم = 5.2 جم كلوريد الصوديوم * (1 مول / 58.44 جم) = 0.8898 مول = 0.09 مول
قسّم 800 مل من الماء على 1000 ، ستحصل على حجم الماء باللتر.
- يمكنك أيضًا ضرب 800 مل في معامل التحويل 1 لتر / 1000 مل من المليلتر إلى اللتر.
- لتقصير عملية الضرب على النحو الوارد أعلاه ، يمكنك إرجاع العلامة العشرية 3 أرقام إلى اليسار.
- الحجم = 800 مل * (1 لتر / 1000 مل) = 800 مل / 1000 مل = 0.8 لتر
اقسم عدد مولات المذاب على حجم المحلول باللترات. لحساب التركيز المولي ، تحتاج إلى قسمة 0.09 مول من المذاب (في هذه الحالة ، NaCl) على حجم المحلول باللترات.
- التركيز المولي = عدد مولات المذاب / عدد لترات المحلول = 0.09 مول / 0.8 لتر = 0.1125 مول / لتر
سجل النتيجة النهائية. قرب النتيجة إلى رقمين أو ثلاثة أرقام بعد الفاصلة واختصر "التركيز المولي" بـ "M" مع الرمز الكيميائي المذاب.
- نتيجة: 0.11 مول كلوريد الصوديوم



