مؤلف:
Clyde Lopez
تاريخ الخلق:
26 تموز 2021
تاريخ التحديث:
1 تموز 2024

المحتوى
- خطوات
- طريقة 1 من 4: حساب النسبة المئوية باستخدام معادلة الوزن / الحجم
- طريقة 2 من 4: تحضير محلول جزيئي
- طريقة 3 من 4: تخفيف حلول التركيز المعروف
- طريقة 4 من 4: الامتثال لاحتياطات السلامة
- نصائح
- تحذيرات
- ماذا تحتاج
يمكن تحضير المحاليل الكيميائية البسيطة بسهولة بعدة طرق في المنزل أو في العمل. سواء كنت تصنع محلولًا من مادة مسحوقية أو تخفف سائلًا ، فمن السهل تحديد الكمية الصحيحة لكل مكون. عند تحضير المحاليل الكيميائية ، تذكر استخدام معدات الحماية الشخصية لتجنب التلف.
خطوات
طريقة 1 من 4: حساب النسبة المئوية باستخدام معادلة الوزن / الحجم
 1 حدد النسبة المئوية المحتوى على وزن/ حجم المحلول. توضح النسب المئوية عدد أجزاء المادة في مائة جزء من المحلول. عند تطبيقه على المحاليل الكيميائية ، فهذا يعني أنه إذا كان التركيز 1 في المائة ، فإن 100 مل من المحلول يحتوي على 1 جرام من المادة ، أي 1 مل / 100 مل.
1 حدد النسبة المئوية المحتوى على وزن/ حجم المحلول. توضح النسب المئوية عدد أجزاء المادة في مائة جزء من المحلول. عند تطبيقه على المحاليل الكيميائية ، فهذا يعني أنه إذا كان التركيز 1 في المائة ، فإن 100 مل من المحلول يحتوي على 1 جرام من المادة ، أي 1 مل / 100 مل. - على سبيل المثال ، بالوزن: يحتوي محلول 10٪ بالوزن على 10 جرامات من المادة المذابة في 100 ملليلتر من المحلول.
- على سبيل المثال ، بالحجم: يحتوي محلول 23 بالمائة بالحجم على 23 مليلترًا من المركب السائل في كل 100 مليلتر من المحلول.
 2 حدد حجم المحلول الذي تريد تحضيره. لمعرفة الكتلة المطلوبة من مادة ما ، يجب عليك أولاً تحديد الحجم النهائي للمحلول الذي تحتاجه. يعتمد هذا الحجم على مقدار الحل الذي تحتاجه ، وكم مرة ستستخدمه ، واستقرار الحل النهائي.
2 حدد حجم المحلول الذي تريد تحضيره. لمعرفة الكتلة المطلوبة من مادة ما ، يجب عليك أولاً تحديد الحجم النهائي للمحلول الذي تحتاجه. يعتمد هذا الحجم على مقدار الحل الذي تحتاجه ، وكم مرة ستستخدمه ، واستقرار الحل النهائي. - إذا كنت بحاجة إلى استخدام محلول جديد في كل مرة ، فقم بإعداد الكمية التي تحتاجها فقط للاستخدام مرة واحدة.
- إذا احتفظ المحلول بخصائصه لفترة طويلة ، يمكنك تحضير كمية أكبر لاستخدامه لاحقًا.
- مثال: تحتاج إلى تحضير محلول كلوريد الصوديوم بنسبة 5٪ بحجم 500 مل.
 3 احسب عدد جرامات المادة المطلوبة لتحضير المحلول. لحساب العدد المطلوب من الجرامات ، استخدم الصيغة التالية: عدد الجرامات = (النسبة المئوية المطلوبة) (الحجم المطلوب / 100 مل). في هذه الحالة ، يتم التعبير عن النسب المئوية المطلوبة بالجرام والحجم المطلوب بالملليلترات.
3 احسب عدد جرامات المادة المطلوبة لتحضير المحلول. لحساب العدد المطلوب من الجرامات ، استخدم الصيغة التالية: عدد الجرامات = (النسبة المئوية المطلوبة) (الحجم المطلوب / 100 مل). في هذه الحالة ، يتم التعبير عن النسب المئوية المطلوبة بالجرام والحجم المطلوب بالملليلترات. - مثال: تحتاج إلى تحضير محلول كلوريد الصوديوم بنسبة 5٪ بحجم 500 مل.
- عدد الجرامات = (5 جم) (500 مل / 100 مل) = 25 جرام.
- إذا تم إعطاء كلوريد الصوديوم كمحلول ، فما عليك سوى تناول 25 مليلترًا من كلوريد الصوديوم بدلاً من جرامات المسحوق وطرح هذا الحجم من الحجم النهائي: 25 مليلترًا من كلوريد الصوديوم إلى 475 مليلترًا من الماء.
 4 وزن المادة. بعد حساب الكتلة المطلوبة للمادة ، يجب قياس هذه الكمية. خذ مقياسًا معايرًا ، ضع وعاءًا عليه واضبطه على الصفر. زن الكمية المطلوبة من المادة بالجرام واسكبها.
4 وزن المادة. بعد حساب الكتلة المطلوبة للمادة ، يجب قياس هذه الكمية. خذ مقياسًا معايرًا ، ضع وعاءًا عليه واضبطه على الصفر. زن الكمية المطلوبة من المادة بالجرام واسكبها. - قبل الاستمرار في تحضير المحلول ، تأكد من تنظيف كفة الميزان من أي بقايا مسحوق.
- في المثال أعلاه ، يجب أن تزن 25 جرامًا من كلوريد الصوديوم.
 5 قم بإذابة المادة بالكمية المطلوبة من السائل. ما لم ينص على خلاف ذلك ، يتم استخدام الماء كمذيب. خذ كوب قياس وقم بقياس الكمية المطلوبة من السائل. ثم قم بإذابة مادة المسحوق في السائل.
5 قم بإذابة المادة بالكمية المطلوبة من السائل. ما لم ينص على خلاف ذلك ، يتم استخدام الماء كمذيب. خذ كوب قياس وقم بقياس الكمية المطلوبة من السائل. ثم قم بإذابة مادة المسحوق في السائل. - قم بتوقيع الحاوية التي ستخزن فيها الحل. حدد المادة بوضوح وتركيزها عليها.
- مثال: قم بإذابة 25 جرامًا من كلوريد الصوديوم في 500 مليلتر من الماء لعمل محلول بنسبة 5٪.
- تذكر أنه إذا كنت تخفف مادة سائلة ، للحصول على الكمية المطلوبة من الماء ، اطرح حجم المادة المضافة من الحجم النهائي للمحلول: 500 مل - 25 مل = 475 مل من الماء.
طريقة 2 من 4: تحضير محلول جزيئي
 1 تحديد الوزن الجزيئي للمادة المستخدمة باستخدام الصيغة. وزن الصيغة (أو الوزن الجزيئي ببساطة) للمركب مكتوب بالجرام لكل مول (جم / مول) على جدار الزجاجة. إذا لم تتمكن من العثور على الوزن الجزيئي على الزجاجة ، فابحث على الإنترنت.
1 تحديد الوزن الجزيئي للمادة المستخدمة باستخدام الصيغة. وزن الصيغة (أو الوزن الجزيئي ببساطة) للمركب مكتوب بالجرام لكل مول (جم / مول) على جدار الزجاجة. إذا لم تتمكن من العثور على الوزن الجزيئي على الزجاجة ، فابحث على الإنترنت. - الوزن الجزيئي للمادة هو كتلة مول واحد من تلك المادة (بالجرام).
- مثال: الوزن الجزيئي لكلوريد الصوديوم (NaCl) هو 58.44 جم / مول.
 2 حدد حجم المحلول المطلوب باللترات. من السهل جدًا تحضير لتر واحد من المحلول ، حيث يتم التعبير عن مولاريته في مولات / لتر ، ومع ذلك ، قد يكون من الضروري إنتاج لترات أكثر أو أقل ، اعتمادًا على الغرض من المحلول. استخدم الحجم النهائي لحساب العدد المطلوب من الجرامات.
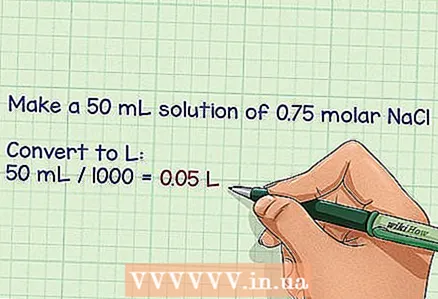
2 حدد حجم المحلول المطلوب باللترات. من السهل جدًا تحضير لتر واحد من المحلول ، حيث يتم التعبير عن مولاريته في مولات / لتر ، ومع ذلك ، قد يكون من الضروري إنتاج لترات أكثر أو أقل ، اعتمادًا على الغرض من المحلول. استخدم الحجم النهائي لحساب العدد المطلوب من الجرامات. - مثال: من الضروري تحضير 50 مل من محلول مع جزء مولاري من كلوريد الصوديوم يبلغ 0.75.
- لتحويل المليلتر إلى لتر ، اقسمها على 1000 واحصل على 0.05 لتر.
 3 احسب عدد الجرامات المطلوبة لتحضير المحلول الجزيئي المطلوب. للقيام بذلك ، استخدم الصيغة التالية: عدد الجرامات = (الحجم المطلوب) (المولارية المطلوبة) (الوزن الجزيئي وفقًا للصيغة). تذكر أنه يتم التعبير عن الحجم المطلوب باللترات ، والمولارية في المولات لكل لتر ، والوزن الجزيئي وفقًا للصيغة بالجرام لكل مول.
3 احسب عدد الجرامات المطلوبة لتحضير المحلول الجزيئي المطلوب. للقيام بذلك ، استخدم الصيغة التالية: عدد الجرامات = (الحجم المطلوب) (المولارية المطلوبة) (الوزن الجزيئي وفقًا للصيغة). تذكر أنه يتم التعبير عن الحجم المطلوب باللترات ، والمولارية في المولات لكل لتر ، والوزن الجزيئي وفقًا للصيغة بالجرام لكل مول. - مثال: إذا كنت تريد تحضير 50 مليلترًا من محلول مع كسر مولاري من كلوريد الصوديوم 0.75 (الوزن الجزيئي وفقًا للصيغة: 58.44 جم / مول) ، يجب أن تحسب عدد جرامات كلوريد الصوديوم.
- عدد الجرامات = 0.05 لتر * 0.75 مول / لتر * 58.44 جم / مول = 2.19 جرام من كلوريد الصوديوم.
- عن طريق تقليل وحدات القياس ، تحصل على جرامات من المادة.
 4 وزن المادة. قم بوزن الكمية المطلوبة باستخدام ميزان تمت معايرته بشكل صحيح. ضع وعاءً على الميزان وصفرًا قبل الوزن. أضف المادة إلى الوعاء حتى تصل إلى الكتلة المطلوبة.
4 وزن المادة. قم بوزن الكمية المطلوبة باستخدام ميزان تمت معايرته بشكل صحيح. ضع وعاءً على الميزان وصفرًا قبل الوزن. أضف المادة إلى الوعاء حتى تصل إلى الكتلة المطلوبة. - نظف كفة الميزان بعد الاستخدام.
- مثال: تزن 2.19 جرام من كلوريد الصوديوم.
 5 قم بإذابة المسحوق بالكمية المطلوبة من السائل. ما لم يذكر خلاف ذلك ، فإن معظم الحلول تستخدم الماء. في هذه الحالة ، يتم أخذ نفس حجم السائل الذي تم استخدامه لحساب كتلة المادة. أضف المادة إلى الماء وحركها حتى تذوب تمامًا.
5 قم بإذابة المسحوق بالكمية المطلوبة من السائل. ما لم يذكر خلاف ذلك ، فإن معظم الحلول تستخدم الماء. في هذه الحالة ، يتم أخذ نفس حجم السائل الذي تم استخدامه لحساب كتلة المادة. أضف المادة إلى الماء وحركها حتى تذوب تمامًا. - وقع على الحاوية مع المحلول. قم بتسمية المذاب والمولارية بوضوح بحيث يمكنك استخدام المحلول لاحقًا.
- مثال: باستخدام دورق (أداة قياس الحجم) ، قم بقياس 50 مل من الماء وقم بإذابة 2.19 جرام من كلوريد الصوديوم فيه.
- حرك المحلول حتى يذوب المسحوق تمامًا.
طريقة 3 من 4: تخفيف حلول التركيز المعروف
 1 حدد تركيز كل محلول. عند تخفيف المحاليل ، يجب أن تعرف تركيز المحلول الأصلي والمحلول الذي تريد الحصول عليه.هذه الطريقة مناسبة لتخفيف المحاليل المركزة.
1 حدد تركيز كل محلول. عند تخفيف المحاليل ، يجب أن تعرف تركيز المحلول الأصلي والمحلول الذي تريد الحصول عليه.هذه الطريقة مناسبة لتخفيف المحاليل المركزة. - مثال: قم بتحضير 75 مل من محلول كلوريد الصوديوم 1.5 مولار من محلول 5 مولار.يحتوي محلول المخزون على تركيز 5 م ومن الضروري تخفيفه إلى تركيز 1.5 م.
 2 أوجد حجم المحلول النهائي. من الضروري العثور على حجم الحل الذي تريد الحصول عليه. سيكون عليك حساب كمية المحلول المطلوبة لتخفيف هذا المحلول إلى التركيز والحجم المطلوبين.
2 أوجد حجم المحلول النهائي. من الضروري العثور على حجم الحل الذي تريد الحصول عليه. سيكون عليك حساب كمية المحلول المطلوبة لتخفيف هذا المحلول إلى التركيز والحجم المطلوبين. - مثال: قم بإعداد 75 مل من محلول كلوريد الصوديوم 1.5 مولار من محلول 5 M. في هذا المثال ، يكون حجم المحلول النهائي 75 مليلترًا.
 3 احسب حجم المحلول المطلوب لتخفيف محلول البداية. للقيام بذلك ، تحتاج إلى الصيغة التالية: V.1ج1= V.2ج2حيث V.1 - حجم المحلول المطلوب ج1 - تركيزه ، V.2 - حجم المحلول النهائي C2 - تركيزه.
3 احسب حجم المحلول المطلوب لتخفيف محلول البداية. للقيام بذلك ، تحتاج إلى الصيغة التالية: V.1ج1= V.2ج2حيث V.1 - حجم المحلول المطلوب ج1 - تركيزه ، V.2 - حجم المحلول النهائي C2 - تركيزه. - لحساب حجم السائل المطلوب ، من الضروري إعادة كتابة المساواة فيما يتعلق بـ V.1: الخامس1 = (الخامس2ج2) / ج1.
- مثال: تحتاج إلى تحضير 75 مل من محلول كلوريد الصوديوم بتركيز 1.5 م من محلول بتركيز 5 م.
- الخامس1 = (الخامس2ج2) / ج1 = (0.075 لتر * 1.5 م) / 5 م = 0.0225 لتر.
- حول اللترات مرة أخرى إلى مليلتر بضربها في 1000 لتحصل على 22.5 مليلتر.
 4 اطرح حجم الحل الأصلي من الحجم النهائي المخطط له. نتيجة لتخفيف المحلول ، من الضروري الحصول على حجم نهائي ثابت. اطرح حجم محلول المخزون من الحجم النهائي لتحديد حجم محلول التخفيف.
4 اطرح حجم الحل الأصلي من الحجم النهائي المخطط له. نتيجة لتخفيف المحلول ، من الضروري الحصول على حجم نهائي ثابت. اطرح حجم محلول المخزون من الحجم النهائي لتحديد حجم محلول التخفيف. - مثال: الحجم النهائي 75 ملليلتر والحجم الأصلي 22.5 ملليلتر. وهكذا نحصل على 75 - 22.5 = 52.5 ملليلترًا. سيكون هذا الحجم من السائل ضروريًا لتخفيف المحلول.
 5 امزج الكمية المحسوبة من محلول المخزون مع سائل التخفيف. باستخدام دورق (أداة لقياس حجم السائل) ، قم بقياس الكمية المطلوبة من محلول المخزون واخلطها مع الحجم المطلوب من سائل التخفيف.
5 امزج الكمية المحسوبة من محلول المخزون مع سائل التخفيف. باستخدام دورق (أداة لقياس حجم السائل) ، قم بقياس الكمية المطلوبة من محلول المخزون واخلطها مع الحجم المطلوب من سائل التخفيف. - مثال: قم بقياس 22.5 مليلتر من محلول مخزون كلوريد الصوديوم 5 مولار وقم بالتخفيف باستخدام 52.5 مليلتر من الماء. حرك المحلول.
- اكتب على الحاوية مع المحلول المخفف تركيزه وتكوينه: 1.5 M NaCl.
- تذكر ، إذا كنت تخفف الحمض بالماء ، يجب أن تضيف حمضًا إلى الماء ، لكن لا تضيف العكس أبدًا.
طريقة 4 من 4: الامتثال لاحتياطات السلامة
 1 استخدم معدات الحماية الشخصية. عند العمل مع المواد الكيميائية والحلول العدوانية ، احمِ من آثارها. تأكد من ارتداء معطف المختبر ، والأحذية المغلقة ، والنظارات الواقية والقفازات.
1 استخدم معدات الحماية الشخصية. عند العمل مع المواد الكيميائية والحلول العدوانية ، احمِ من آثارها. تأكد من ارتداء معطف المختبر ، والأحذية المغلقة ، والنظارات الواقية والقفازات. - استخدم معطف مختبر مصنوع من مادة غير قابلة للاحتراق.
- يجب أن تحتوي نظارات السلامة على دروع جانبية تغطي العينين من الجانب.
 2 العمل في منطقة جيدة التهوية. عندما تختلط المحاليل ، يمكن إطلاق غازات متطايرة. يجب التعامل مع بعض المواد فقط تحت غطاء المختبر. إذا كنت تقوم بخلط الحلول في المنزل ، فافتح النوافذ وقم بتشغيل مروحة لضمان دوران الهواء الكافي.
2 العمل في منطقة جيدة التهوية. عندما تختلط المحاليل ، يمكن إطلاق غازات متطايرة. يجب التعامل مع بعض المواد فقط تحت غطاء المختبر. إذا كنت تقوم بخلط الحلول في المنزل ، فافتح النوافذ وقم بتشغيل مروحة لضمان دوران الهواء الكافي.  3 أضف الحمض إلى الماء. عند تخفيف الأحماض المركزة ، قم دائمًا بإضافة الحمض إلى الماء. عندما يتم خلط الماء والحمض ، يحدث تفاعل طارد للحرارة (مع إطلاق الحرارة) ، والذي يمكن أن يؤدي إلى انفجار إذا تمت إضافة الماء إلى الحمض ، وليس العكس.
3 أضف الحمض إلى الماء. عند تخفيف الأحماض المركزة ، قم دائمًا بإضافة الحمض إلى الماء. عندما يتم خلط الماء والحمض ، يحدث تفاعل طارد للحرارة (مع إطلاق الحرارة) ، والذي يمكن أن يؤدي إلى انفجار إذا تمت إضافة الماء إلى الحمض ، وليس العكس. - تذكر احتياطات السلامة في كل مرة تعمل فيها مع الأحماض.
نصائح
- قبل البدء ، تعرف على الموضوع. المعرفة قوة!
- جرب استخدام المنتجات المنزلية العادية. لا تحاول أن تفعل أي شيء غير عادي. إذا كنت تشك في احتمال ظهور خطر ، فاستسلم.
تحذيرات
- لا تخلط المبيض والأمونيا.
- استخدم معدات السلامة والنظارات الواقية والمريلة البلاستيكية والقفازات المصنوعة من النيوبرين حسب الحاجة.
ماذا تحتاج
- موازين ميكانيكية أو إلكترونية دقيقة لتحديد الكتلة. على سبيل المثال ، يمكنك استخدام ميزان المطبخ.
- تخرج الأواني الزجاجية. يمكن العثور على هذه الأواني في متجر أدوات المطبخ أو طلبها عبر الإنترنت. يأتي زجاج القياس في مجموعة متنوعة من الأشكال والأحجام. ستعمل الأطباق البلاستيكية ، رغم أنها لن تتحمل درجات الحرارة العالية.